프로세사 파마슈티컬스: 시총 2천만 달러, 그러나 FDA와 30번 승인을 만든 사람들
2025년 6월 17일, 세상은 두 개의 공시를 동시에 목격했습니다.
Processa Pharmaceuticals가 4억 5천만 달러 규모의 라이선싱 계약을 체결했다는 소식과, 같은 날 생존을 위해 700만 달러를 증자했다는 발표였습니다.
주가는 0.36달러, 시가총액은 고작 2천만 달러.
도대체 왜 FDA 승인 30건의 경력을 가진 팀이 이토록 작은 배를 타고 있는 걸까요.

프로세사 파마슈티컬스: 이미 승인된 항암제를 '다시 쓰는' 연금술
2017년, 약학 박사 David Young은 한 가지 질문을 던지며 이 회사를 시작했습니다.
"카페시타빈처럼 이미 FDA 승인을 받은 항암제를, 왜 우리는 그대로 쓰고 있을까?"
그가 발견한 진실은 충격적이었습니다.
전 세계에서 가장 널리 쓰이는 유방암 치료제 카페시타빈은, 체내에서 약물의 75-85%가 암을 죽이지 못하고 부작용만 일으키는 쓸모없는 대사물로 변한다는 것이었습니다.
David Young의 답은 명확했습니다.
기존 항암제의 화학 구조는 그대로 두되, 체내에서 약물이 대사되는 방식만 바꾸는 것입니다.
이것이 Processa의 Next Generation Cancer (NGC) 플랫폼의 시작이었습니다.
David Young과 Sian Bigora는 지난 30년간 FDA와 함께 규제 과학 가이드라인을 만들고, 30건 이상의 FDA 승인을 이끌어낸 전설적인 인물들이었습니다.
프로세사 파마슈티컬스: 카페시타빈을 5-10배로 뒤집은 비밀 병기
기존 카페시타빈은 체내에서 10-20%만 암세포를 죽이는 활성 물질로 변했지만, NGC-Cap은 80-90%가 암세포를 죽이는 활성 물질로 변합니다.
Phase 1b 임상에서 NGC-Cap은 기존 카페시타빈 대비 5-10배 높은 항암 효과를 보였습니다.
그런데 부작용은 오히려 줄어들었습니다.
손발 괴사 부작용은 기존 50%에서 단 6%로 감소했고, 말기 위장관암 환자 12명 중 8명이 부분 관해 또는 안정 상태를 보였습니다.
2024년 10월부터 시작된 Phase 2 임상시험은 현재 전 세계 30개 병원에서 진행 중이며, 올해 하반기 중간 분석 결과가 발표될 예정입니다.
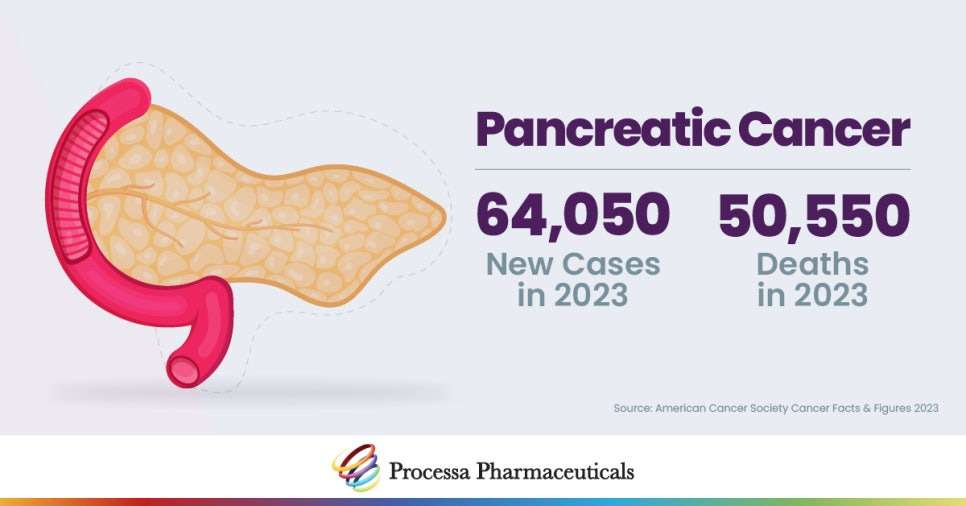
두 번째 파이프라인 NGC-Gem은 젬시타빈 내성 췌장암 환자들에게, 세 번째 NGC-Iri는 종양/근육 비율 200배로 블랙박스 경고를 지울 잠재력을 보여줍니다.

프로세사 파마슈티컬스: 4억 5천만 달러 뒤에 숨은 잔혹한 현실
6월 17일의 Intact Therapeutics 계약 조건은 화려했지만, Processa는 이 돈의 60%를 원 라이선서와 나눠야 하고, 당장 들어오는 현금은 250만 달러뿐입니다.
2024년 전체 매출은 0달러, 순손실은 1,288만 달러, 현금은 694만 달러에 불과합니다.
주가는 52주 최고가 1.50달러에서 0.15달러까지 떨어졌다가 현재 0.36달러입니다.
직원은 단 10명입니다.
그러나 이 10명의 팀은 FDA 승인 30건 이상의 경력을 가지고 있고, FDA 가이드라인을 만든 사람들입니다.
임상 실패 리스크, 자금 고갈 리스크, 그리고 희석 리스크가 모두 현실화될 수 있는 상황입니다.

프로세사 파마슈티컬스: 올해 하반기, 운명이 결정된다
Processa의 운명은 올해 하반기 NGC-Cap Phase 2 중간 분석에 달려 있습니다.
만약 데이터가 긍정적이라면, 대형 제약사 파트너십이 열릴 것입니다.
유방암 치료 시장은 연간 300억 달러 이상이고, 5-10배 효과 개선과 부작용 감소가 입증된다면 이것은 게임 체인저입니다.
Processa는 새로운 약을 만드는 것이 아니라, 이미 검증된 약을 더 안전하고 효과적으로 만드는 전략을 택했습니다.
이것은 실패 확률을 낮추고, FDA 승인 경로를 단축시킵니다.
그리고 이 팀은 그 길을 30번 이상 걸어온 사람들입니다.
Processa는 지금 절벽 끝에 서 있습니다.
이 작은 회사의 다음 카드가 무엇인지, 그것이 역사를 쓸 수 있을지 지켜보는 것이 이 드라마의 진짜 의미입니다.
7380 Coca Cola Drive, Suite 106
Hanover, Maryland 21076
United States
#ProcessaPharma #PCSA #NGCCap #NGCGem #NGCIri #카페시타빈 #FDA승인 #IntactTherapeutics #항암제개선 #NextGenerationCancer

[월가초딩 생각]
한 번도 어렵다는 FDA 승인 30번 이상 받은 연구팀이라면 어마어마한 실력자들이네요.
완전히 새로운 약이 아니라 이미 검증된 약을 개선하는 전략을 택했다는 것도 신선해요.
쉬운 길이라고 생각될 수 있지만, 실패 확률을 낮추는 현명한 접근이에요.
하지만 현실이 가혹하네요. 임상 결과가 모든 것을 좌우할 것 같아요.
Q1. NGC-Cap의 Phase 2 중간 분석이 긍정적이라고 해도, Processa가 독자적으로 Phase 3까지 진행할 자금력이 있을까요?
Q2. 이 팀이 FDA 승인 30건의 경력을 가지고 있다면, 왜 이렇게 작은 회사에서 일하고 있을까요?